SEPSIS
ABDOMINAL
Inicialmente se define como:
- Contaminación abdominal la cual indica la existencia de microorganismos a nivel peritoneal lo cual ocurre antes de que exista invasión tisular.
- Infección intraabdominal la cual hace referencia a la respuesta inflamatoria local existente debida a la invasión del tejido.
EPIDEMIOLOGÍA
En la revisión realizada se
evidenciaron datos estadísticos a nivel nacional encontrando que existen dos
causas que condicionan la existencia de una sepsis intraabdominal las cuales
son:
- Apendicitis aguda: causa que condiciona aproximadamente 20 ingresos anuales a cirugía de tipo gastrointestinal, encontrando que existe un 3,5 en mortalidad en pacientes con apendicitis.
- Perforación intestinal: es otro de los casos que conlleva a una sepsis abdominal debido a procesos febriles que generalmente presenta complicaciones entre un 7-21% de todos los casos.
Las infecciones a nivel
intraabdominal se pueden presentar por diferentes formas:
- . Manera espontánea: La cual es causada por un número imitado de bacterias especialmente se evidencia en pacientes con ascitis. Esta infección se puede tratar únicamente con antibiótico.
- . Infección de la cavidad peritoneal: esta se presenta como una peritonitis o absceso localizado originado en pacientes críticos con una peritonitis secundaria.
- . Peritonitis: representa un síndrome de respuesta inflamatoria asociada a estímulos infecciosos o no infecciosos.
| ETIOLOGÍA
Las enfermedades de duodeno
o de estómago alteran la flora intestinal generando la obstrucción del yeyuno e
íleon ocasionando estasis lo cual genera el aumento de bacterias como los
anaerobios y coliformes que se encuentran en el intestino delgado. La sepsis
intraabdominal presenta inicialmente peritonitis aguda debido a la bacteria
faculativa encontrando que los pacientes que pasan esta fase tienden a generar
abscesos anaerobios de la bacteria bacteroides fragilis.
CUADRO
CLINICO
- Dolor abdominal: el cual se acompaña de fiebre, náuseas y vomito este cuadro puede evolucionar a choque dependiendo al tipo de bacterias que existan en un tiempo dado. Este dolor también está asociado a la cantidad de jugo gástrico. Se evidencia que el dolor inicial es de baja intensidad hasta cuando existe la multiplicación bacteriana la cual da como resultado sustancias irritantes. debido a la peritonitis se puede evidenciar que estos pacientes se encuentran en cama para evitar al máximo los movimientos.
- Espasmo reflejo tónico de la musculatura abdominal: el cual se presenta en la zona más comprometida, donde la intensidad del espasmo se ve acompañada de inflamación peritoneal la cual depende de la fase inflamatoria y la velocidad con la que esta se desarrolle, este espasmo muscular es un apéndice perforado que puede encontrarse mínimo o ausente.
Diagnostico
- Cultivos anaeróbicos
- Sensibilidad de placas abdominales y torácicas (detectar sepsis intraabdominal).
- Ultrasonografía implementada para confirmar presencia de absceso intrabdominal
- Tomografía computada para evidenciar la existencia de lesiones fuera del área sospechada.
PANCREATITIS
AGUDA
Es una enfermedad inflamatoria que compromete
el páncreas y a tejidos vecinos, donde su presentación clínica es variable y
tiene un porcentaje de morbilidad importante, para su diagnóstico se requiere
que sea precoz y de manejo oportuno para evitar así las complicaciones e
incluso la muerte.
Fases
- . Inflamatoria : donde el tratamiento de sostén es prioritario.
- . Necrosis pancreática: el cual da lugar a complicaciones sistémicas produciendo infección en el tejido necrosado dando como resultado la translocación de gérmenes entéricos. Esta necrosis esta fuertemente predisponente a falla multiorganica en un 35%.
PERITONITIS
SECUNDARIA
Es la forma más frecuente originada
en procesos intraperitoneales en cual inicia como una peritonitis localizada y
puede ir evolucionando hasta extenderse a todo el peritoneo. Encontramos una
peritonitis terciaria esta es una forma de peritonitis secundaria la cual puede
continuar como un síndrome de respuesta inflamatoria sistémica asociada a
infección peritoneal.
La progresión de la
infección dependerá del grado de vulnerancia y de las defensas con las que
cuente el paciente. Se produce un mecanismo con un proceso exudativo
encontrando tres formas de padecimiento que son:
1 Fuente de inoculación la
cual no persiste por ser bloqueada por el exudado y fibrina lo cual puede
retrogradar el proceso inflamatorio.
2 El proceso inflamatorio
infeccioso da lugar a la peritonitis localizada donde el proceso queda
bloqueado por adherencias laxas y luego se fibrosa.
MANIFESTACIONES
SISTÉMICAS O GENERALES
Cardiovasculares: En los
cuadros graves se tiene hipovolemia que está dada por la importante pérdida de
fluidos por los exudados, falta de aportes de líquidos y a la sustracción de
estos por el íleo intestinal. La hipovolemia junto con el shock séptico lleva a
una falla cardiovascular con disminución del débito cardíaco y falta de
oxigenación tisular que lleva a una acidosis respiratoria.
Respiratorios: Existen
varios mecanismos que llevan a una disminución de la función respiratoria y que
pueden actuar en distinto grado, en el caso de la motilidad diafragmática esta
disminuida o ausente por el dolor y vecindad de la infección lo que lleva a la
producción de atelectasias especialmente en las bases y derrames pleurales. El
edema de la membrana alveolocapilar y las alteraciones de las presiones
capilares por los cambios cardiovasculares disminuyen la función pulmonar.
Renales: La acción directa de las toxinas y la falta de
una buena perfusión por falla cardiovascular llevan a una insuficiencia renal,
cuando la presión intraabdominal supera los 30 mmHg (Síndrome compartimental
del abdomen) la perfusión renal y filtrado glomerular se ven reducidos y
aparecen efectos mecánicos directos sobre la circulación esplácnica con
hipoperfusión que condiciona trastornos gastrointestinales, hemorragia
digestiva por isquemia mucosa, permeabilidad de toxinas y traslocación
bacteriana.
EMBARAZO
ECTÓPICO:
Es la anidación y desarrollo
del óvulo fecundado fuera de la cavidad endometrial, en las últimas 3 décadas
su incidencia ha aumentado, ha disminuido su morbimortalidad y es la primera
causa de mortalidad en el primer trimestre de embarazo, asociándose a otra
nueva gestación en el 50% de los casos, de los cuales el 30- 50% concluyen con
el parto de un feto vivo. Por todo ello, su sospecha precoz por el médico de
Atención Primaria y el ginecólogo es trascendental, ante toda mujer en edad
fértil con:
1) Factores de riesgo para
gestión extrauterina (GE) (enfermedad inflamatoria pélvica, cirugía tubárica,
dispositivo intrauterino, EE previo, tabaquismo, endometriosis,
cromosomopatías, fecundación asistida, inducción de la ovulación.
2) Síntomas típicos (amenorrea, abdominalgia,
metrorragia, síntomas generales de gestación náuseas y vómitos, e incluso
síncope y shock.
INFECCIONES
INTRA-ABDOMINALES
La superficie total del
peritoneo es de 1,7 m2, estéril y contiene 50 mililitros de un líquido de color
amarillo claro.
El peritoneo consta de una
sola capa de células mesoteliales (Células Mesoteliales Peritoneales, CMP),
sostenidas en una membrana basal sobre un lecho de tejido conjuntivo, formado a
su vez por células adiposas, macrógafos, fibroblastos, linfocitos y algunas
fibras de colágeno. Las CMP pueden expresar en su superficie marcadores que les
permiten:
a) Promover la marginación y
migración de neutrófilos.
b) Interactuar con la matriz extracelular
proteínica.
c) Presentar antígenos a las células
inmunitarias.
d) Producir biológicamente moléculas
importantes como citoquinas proinflamatorias (IL-6, IL-8 FNT alfa), óxido
nítrico, factores de crecimiento, activador del plasminógeno tisular, e
inhibidor del activador del plasminógeno, para así mismo combatir la
colonización y eliminar elementos extraños.
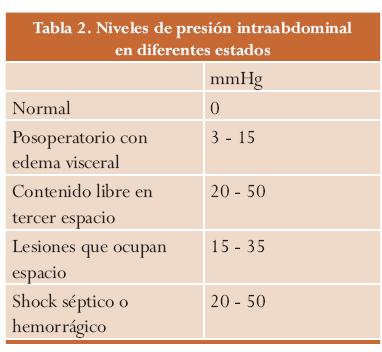
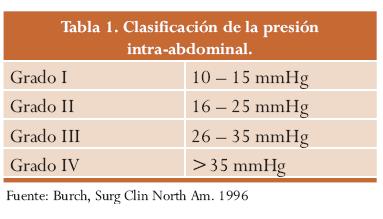
HIPERTENSIÓN
INTRA-ABDOMINAL Y SÍNDROME COMPARTIMENTAL ABDOMINAL
La Hipertensión
Intra-Abdominal (HIA) se refiere sólo a una medida de presión elevada. Cuando
ese aumento de la Presión Intra-Abdominal (PIA) se acompaña de disfunción
progresiva generalizada se habla del Síndrome Compartimental Abdominal (SAC).
La expansión del contenido
intraabdominal puede deberse a diversas causas o a la combinación de ellas,
entre las cuales tenemos:
1. Líquidos como sangre (por
cirugía o trauma), exudado por peritonitis, trasudado por disfunción endotelial
o hepática (pre-eclampsia, síndrome HELLP), de un tercer espacio producto de
reanimación excesiva o pérdida capilar (preeclampsia por disminución de presión
oncótica).
2. Distensión de órganos de
capacitancia (íleo de diversas causas, obstrucción intestinal en todas sus formas,
útero grávido y visceromegalias benignas o malignas).
3. Lesiones o cuerpos que
ocupan espacio (masas y neoplasias abdominales, hematomas contenidos o
empaquetamiento abdominal).
4. Pérdida de elasticidad
del componente abdominal (fajas abdominales manejadas por enfermería, el cierre
prematuro o inadecuado en correcciones de la pared abdominal en hernias o
evisceraciones, escaras o cicatrices retráctiles o quemaduras).
5. Acumulación de gas libre
dentro de la cavidad abdominal (neumoperitoneo quirúrgico).
En la fisiopatología del
síndrome compartimental abdominal es vital considerar alteraciones en los
siguientes sistemas:
Cardiovascular: se
evidencian cambios con elevaciones de la PIA superiores a 25 mmHg, estos
cambios se inician con la desviación cefálica del diafragma, incremento de la
presión intratorácica, y sobre presión en los vasos venosos, como la vena cava
inferior y vena porta.
Pulmonar: ante la presencia de una PIA mayor de 16 mm Hg se produce
elevación del diafragma e incapacidad de la musculatura torácica para actuar,
hay compresión del parénquima pulmonar y desarrollo de disfunción pulmonar. En
casos de shock hipovolemico o coagulopatía e hipotensión, se puede producir
atelectasia pulmonar, caída del transporte de gases transmembrana e incremento
del shunt intrapulmonar.
Renal: al disminuir la
presión de perfusión renal hay una caída directa de la tasa de filtración
glomerular con PIA por encima de 15 mm Hg y anuria con PIA superior a 30 mm Hg.
Estos cambios parecen reversibles al descomprimir la cavidad abdominal.
Gastrointestinal: la disminución del flujo mesentérico con PIA por
encima de 10 mm Hg promueve la compresión de las paredes de las venas
mesentéricas, produciendo hipertensión venosa y edema de asas.
Presión intracraneana: se ha encontrado que presiones por encima de 25
mm Hg disminuyen de forma significativa la perfusión cerebral.35 Se propone que
el aumento de la PVC a causa del incremento de la PIA
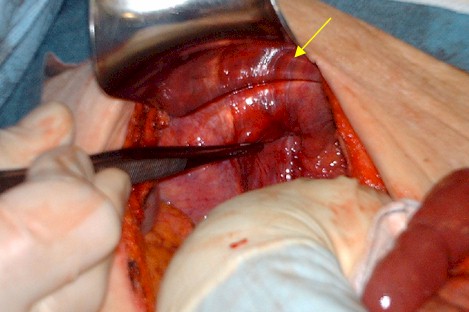
CIRUGÍA
DE ABDOMEN ABIERTO EN GINECO OBSTETRICIA
PROTOCOLO DE VENTILACIÓN MECÁNICA
1.
Preparación del ventilador.
En
la la preparación del ventilador debe ser realizado previa a la conexión del
paciente a éste, idealmente previo incluso a la manipulación de la vía
aérea.
Los parámetros a fijar son:
a)
volumen corriente
b) PEEP
c) frecuencia respiratoria (FR)
d) FiO2, y e)
flujo o tiempo inspiratorio.
El volumen corriente o también llamado
volumen tidas (Vt) puede oscilar entre 6 y 10 ml/kg al principio
del inicio de la ventilación mecanica
debe tenerse en cuenta que es menor mientras mayor compromiso del
parénquima pulmonar tenga el paciente (SDRA). La ventilación controlada por
volumen es el modo ventilatorio ideal para cuando se inicia la ventilación
mecánica, por cuanto podemos evaluar rápidamente la mecánica ventilatoria del
paciente y detectar problemas existentes. (Bugedo,
G, Bruhn, A. (2012).)
La
PEEP (presión positiva
al final de la expiración) debe aplicarse a todo paciente en ventilación
mecánica. Todos los pacientes que
requieren un soporte ventilatorio, bien sea por la patología de base o por el
efecto de los medicamentos sedantes y/o relajantes tienen una disminución de su
capacidad residual funcional que genera el colapso alveolar, cortocircuito
pulmonar e hipoxemia. (Bugedo, G, Bruhn, A. (2012).)
La
FiO2 debe estar en 1.0 cuando se inicia la ventilación
mecánica, para revertir rápidamente la hipoxemia que presentaba el paciente, o
si ha habido problemas durante la intubación.
Dentro de los primeros 30 minutos debiéramos intentar disminuir la FiO2
bajo 0.6, de modo de disminuir la toxicidad por O2 y las atelectasias por uso
de altas FiO2. Sin embargo, este es un
tema controvertido, y mientras no tengamos una saturación sobre 90%, la FiO2
debe mantenerse elevada hasta descartar otras complicaciones.
La
frecuencia respiratoria (FR) debe ajustarse para normocapnia,
idealmente apoyada con un capnógrafo. La
FR inicial se debe aplicar de 10 a 20 ciclos/min, mayor mientras más
taquipneico estaba el paciente previo a la conexión al ventilador. La PaCO2 no es un objetivo fundamental
durante la ventilación mecánica, y no se tendra claridad cómo impacta la
evolución del paciente. Sin embargo,
hipocapnia marcada (bajo 32 o 35 mmHg) no son recomendables, excepto en
pacientes con edema cerebral e hipertensión intracraneana refractaria a las
medidas iniciales de manejo. Por otra
parte pacientes con SDRA severo pueden tener PaCO2 (por sobre) > 60 mmHg bien
toleradas y que sólo denotan la gravedad del compromiso pulmonar. Así, PaCO2 entre 35 y 50 mmHg debiera ser
nuestra meta en la mayoría de los pacientes.
El
flujo inspiratorio, tiempo inspiratorio y relación I:E, está
relacionados, y también con la frecuencia respiratoria. En algunos ventiladores, programamos Vt, FR y
relación I:E, siendo el flujo una variable dependiente
2.
Inicio de la ventilación mecánica.
Una vez conectado el
paciente al ventilador, se debe observar rápidamente lo adecuado de la
ventilación y de su saturación periférica (oximetría de pulso). Para evaluar la ventilación se ausculta al paciente, observamos la
expansión torácica, miramos la curva del capnógrafo, y las curvas de presión y
flujo en función del tiempo en el ventilador.
Si el paciente no mejora la
oxigenación pese a una adecuada
ventilación se deben descartar algunas causas como neumotórax u ocupación
pleural de otro origen, atelectasias, obstrucción bronquial, secreciones
bronquiales, hipertensión abdominal, tromboembolismo pulmonar, mala perfusión
sistémica (shock), o que el paciente presenta una falla respiratoria severa
(SDRA). La medición de gases arteriales
y la radiografía de tórax nos puede orientar hacia el trastorno
fisiopatológico subyacente, pero pueden
tener demora antes de disponer de sus resultados.
3. Sedación:
No se puede ni debe mantener un paciente con angustia
o agitado, con el argumento que la sedación produce compromiso
hemodinámico. En ese caso, se debe
apurar el aporte de fluídos o inicar noradrenalina, siguiendo el protocolo de
reanimación. Habitualmente, la depresión
hemodinámica secundaria a la presión positiva o la sedación responde a fluídos
y dosis bajas de noradrenalina (<0.1 µg/kg/min). En caso contrario, se debe sospechar
fuertemente un estado de shock.
4. Mecánica Ventilatoria
Una de las ventajas de la
ventilación controlada por volumen a flujo continuo es que tiene la posibilidad
de evaluar fácilmente la mecánica ventilatoria, y algunas complicaciones como
obstrucción bronquial o del tubo endotraqueal, o deterioros bruscos en la
distensibilidad estática, que pueden deberse a complicaciones intercurrentes
(intubación monobronquial, neumotórax, etc).
Los parámetros a medir son presiones
pico, meseta, y presión media de vía aérea.
TRATAMIENTO FISIOTERAPEUTICO
MOVILIDAD PASIVA: este tipo
de movilidad consiste en movimientos realizados dentro de los límites posibles
de la articulación, ya que mantienen los rangos de movilidad, evitan las
contracturas articulares y modulan el tono muscular. Además de que contribuye a
la conductancia vascular hacia los músculos de tipo esquelético.
MOVILIDAD ASISTIDA: son
movimientos producidos sin restricción de un segmento, que se produce por la
contracción activa de los músculos que sobrepasan una articulación, la fuerza
externa proporciona ayuda de tipo mecánica o manual, debido al que el músculo
agonista necesita un tipo de ayuda para completar el movimiento.
Para la
aplicación de estas estrategias deben ir encaminadas a la recuperación
funcional del usuario manejando aspectos que posibilitan la adopción de
posturas, realizar traslados y desplazamientos, lo que se denomina movilización
temprana.
MOVILIZACIÓN TEMPRANA: se
considera que su aplicación disminuye el nivel de fatiga muscular y el
incremento de la fuerza en las extremidades y reduce el tiempo de estancia en
UCI y mayor posibilidad de retorno al estado funcional previo al ingreso a la
unidad.
ELECTROESTIMULACIÓN: la
estimulación eléctrica neuromuscular (NEMS) con grandes beneficios según
estudios desarrollados, dentro de ellos la preservación de la masa muscular,
reducción significativa en los niveles de debilidad adquirida en el medio,
prevención de complicaciones como la polineuropatía y menor duración en el
destete de la ventilación mecánica.
Su
funcionamiento se da por la contracción muscular generada a través del nervio o
de estímulos musculares, dentro de estos los estímulos musculares para los
nervios sensitivos ayudando al tratamiento del dolor, y para crear un campo
eléctrico en los tejidos biológicos simulando o alterando los procesos de
curación y para crear un campo eléctrico en la superficie de la piel para
conducir iones beneficioso para los procesos de curación en o a través de la
piel.
Se identifican beneficios en
4 niveles que son el celular, tisular, segmental y sistemático. Los efectos a
nivel celular pueden ser: excitación de las células nerviosas, cambios en la
permeabilidad de la membrana celular, síntesis proteica, estimulación de
fibroblastos y osteoblastos y modificación de la microcirculación; a nivel
tisular se requieren múltiples eventos celulares para generar: contracción del
musculo esquelético, contracción del musculo liso y regeneración tisular; a
nivel segmental involucra efectos regionales de los dos niveles anteriores.
También ocurre: modificación
de la movilidad articular, bombeo muscular que genera cambios circulatorios y
de actividad linfática, alteración del sistema micro vascular sin estar
asociado al bombeo muscular, un incremento de la movilidad de proteínas hacia
el sistemas linfático con el incremento de la presión oncótica que incrementa
la cantidad de fluido en el sistema linfático, lo que conduce a una mayor
contracción linfática como resultado del aumento del flujo.
A lo anterior se le suma que
la estimulación sensorial de manera indirecta pueda activar el sistema
autonómico, por lo cual se considera posible que se liberen sustancias
adrenérgicas que favorecen la contracción del músculo liso linfático, teniendo
efectos analgésicos por liberación de supresores endógenos del dolor que actúan
en diferentes niveles de su control, efectos analgésicos por la estimulación de
algunos neurotransmisores que controlan la actividad neural en presencia de
estímulos dolorosos.
En fases más avanzadas:
EJERCICIOS
RESPIRATORIOS:
Respiración
abdominal diafragmática: Se realiza en decúbito supino, relajando
los músculos intercostales y accesorios. Se facilita doblando las rodillas.
Deben realizarse inspiraciones profundas, observando que la pared abdominal se
desplaza hacia arriba y desciende el diafragma Para ser efectivo, la inspiración
debe durar 3 segundos.
Respiración
abdominal diafragmática: Inicialmente debe realizarse con la
ayuda de un fisioterapeuta. Una vez aprendido, puede hacerlo el paciente solo
supervisado.
Ejercicios de labios fruncidos: Pueden y deben asociarse al anterior. Se realizan
inspiraciones profundas y espiraciones prolongadas con los labios fruncidos.
Produce disminución del colapso alveolar por incremento de la presión
intraluminal.
AYUDAS MECÁNICAS:
Espirometría incentiva: Constituye
un medio de estimular y monitorizar las inspiraciones profundas en pacientes no
intubados. El paciente realiza múltiples inspiraciones máximas y sostenidas, de
manera voluntaria y a través de un aparato que le permite comprobar la magnitud
de cada inspiración.
Presión
positiva continúa en las vías aéreas (CPAP, BIPAP): Es
un método artificial para mantener abiertas las vías aéreas. Sirve para impedir
y contrarrestar el cierre de vías aéreas y facilitar la ventilación colateral
(movimiento de aire en segmentos pulmonares adyacentes), con lo que se
incrementa la CRF. Puede utilizarse tanto en el paciente intubado como en el no
intubado. Los efectos hemodinámicos y pulmonares son similares a los observados
con la aplicación de PEEP, que no se comentan al no ser motivo del tema y ser
de sobra conocidos.
DISMUCIÓN DEL TRABAJO RESPIRATORIO
Descanso
y disminución del stress: Durante el periodo postoperatorio el
paciente debe tener un ambiente de tranquilidad que le permita disfrutar de
reposo y descanso, no debiendo verse atosigado por la necesidad de realizar
ejercicios respiratorios.
Posición
a 30º: Ya se ha mencionado que en esta posición se evita la
compresión del diafragma por las vísceras abdominales, permitiendo su mejor
desplazamiento, de manera que disminuye el trabajo espiratorio a realizar por
el paciente.
Ayudas
mecánicas: CPAP, BIPAP, PIB: Además de contribuir a
reexpandir el pulmón, contribuyen al trabajo respiratorio al
facilitar la inspiración y disminuyendo o impidiendo la aparición de fatiga
muscular respiratoria.
BIBLIOGRAFÍA
·
Forero,
J. C., & Rodríguez, J. A. (2005). Cirugía de abdomen abierto en
gineco-obstetricia: indicaciones, técnica y manejo. Rev Colomb Obstet
Ginecol, 56, 155–165.
·
González-Ojeda, A., & Velazquez-Ramírez,
G. A. (2005). Peritonitis secundaria. Revista de Investigación Clínica, 57(5),
706–715.
·
López-Luque, P. R., Bergal-Mateo, G. J.,
& López-Olivares, M. C. (2014). El embarazo ectópico: su interés actual en
Atención Primaria de Salud. SEMERGEN - Medicina de Familia, 40(4),
211–217. http://doi.org/10.1016/j.semerg.2013.11.007
·
Onieva, F. G., Fernández, J., Pérez, D.,
Espada, M. J., Jiménez, J. L., & Blanco, G. (2014). Management of emphysematous necrotizing pancreatitis. Revista
Colombiana de Cirugía, 29(1), 59–67.
·
Pérez, J. P. C. (2002). Sepsis abdominal. Retrieved from http://www.medigraphic.com/pdfs/medcri/ti-2002/ti024c.pdf
·
Schwaner, J., Rivas, F., Cancino, A., Torres,
O., Briceño, C., & Riquelme, F. (2003). Pancreatitis aguda: Indice de
severidad en tc. Evaluación de complicaciones y hospitalización. Revista
Chilena de Radiología, 9(4), 187–193.
- Bugedo,
G y Bruhn, A. (2012). PROTOCOLO DE VENTILACION MECANICA. Departamento de
Medicina Intensiva, Pontificia Universidad Católica de Chile recuperado en
https://www.google.com.co/url?sa=t&rct=
j&q=&esrc=s&source=web&cd=1&cad=rja&uact=8&ved=0ahUKEwjKrqm1yajMAhWCwiYKHZ-PDkkQFggbMAA&url=http%3A%2F%2Fescuela.med.puc.cl%2Fdeptos%2Fintensivo%2Fprotocolos%2Fprotocolo%2520VM.doc&usg=AFQjCNGv3PDZqrYld74dROxUonc_EtOxUw&sig2=uyXQZoMe43pWmT9QNmDmyg.
[en línea]. El dia 24 de abril de 2016.
- Bernales, A.
(2011). Spontaneous ventilatory modes on
mechanical ventilation and ICU benefits. Revista
Biomédica Revisada Por Pares. 11(04); 59-100
- Soler,
C. (2015). ESTUDIO DE LA PRESION INTRA-ABDOMINAL EN PACIENTES CRITICOS
VENTILADOS SIN OTRO RIESGO APARENTE DE HIPERTENSION ABDOMINAL. Instituto
Superior de Ciencias Médicas de la Habana Facultad de Ciencias Médicas
“Finlay – Albarrán” Ciudad de La Habana, Cuba.
- Lamsfus,
J. (2014). Ventilación pulmonar protectora durante la cirugía abdominal
mayor: Estudio IMPROVE. New England Journal of Medicine 13 (369): 428-37.
- Larriva,
M et al. (2012). Ventilación por presión vs ventilación por volumen y su
impacto en el nivel de CO2 expirado en una cirugía laparoscópica. Revista
meicana de anestesiología. 35 (3); 181-185
- Perme C, Chandrashekar R. Early mobility and
walking program for patients
- in intensive care units: creating a standard of
care. Am J Crit Care Off Publ Am Assoc Crit-Care Nurses (3):212–21.
- Nava S.
Rehabilitation of patients admitted to a respiratory intensive care
- unit. Arch Phys Med Rehabil. (7):849–54.




No hay comentarios.:
Publicar un comentario